 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298.15K时,EΘ(Sn4+/Sn2+)=0.15V,EΘ(Fe3+/Fe2+)=0.771V,则反应Sn2++2Fe3+=Sn4++2Fe2+的KΘ=(
已知298.15K时,EΘ(Sn4+/Sn2+)=0.15V,EΘ(Fe3+/Fe2+)=0.771V,则反应Sn2++2Fe3+=Sn4++2Fe2+的KΘ=()。
A.9.650×109
B.3.0×1010
C.9.54×1020
D.9.1×10-20
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

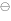 (Fe
(Fe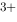 / Fe
/ Fe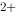 )=0.771V,φ
)=0.771V,φ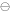 (Ag
(Ag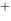 / Ag)=0.7996V,则Ag+Fe
/ Ag)=0.7996V,则Ag+Fe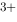 =Ag
=Ag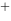 +Fe
+Fe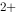 的标准平衡常数为( )。
的标准平衡常数为( )。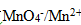 的标准电极电位φ=1.51V,当pH=3.0 时,它的条件电位为( )
的标准电极电位φ=1.51V,当pH=3.0 时,它的条件电位为( )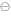 (Fe
(Fe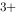 / Fe
/ Fe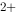 )=0.771V,φ
)=0.771V,φ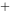 / Ag)=0.7996V,则Ag+Fe
/ Ag)=0.7996V,则Ag+Fe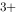 =Ag
=Ag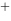 +Fe
+Fe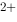 的标准平衡常数为( )。
的标准平衡常数为( )。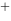 = Zn
= Zn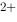 + 2Ag处于标准状态的电池电动势为( )。
+ 2Ag处于标准状态的电池电动势为( )。 (Ag
(Ag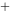 /Ag) - φ
/Ag) - φ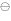 (Zn
(Zn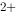 /Zn)
/Zn)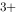 (1 mol·L
(1 mol·L )‖Ag
)‖Ag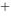 (1 mol·L
(1 mol·L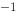 )︱Ag(+)中,若向银半电池中加入适量的NaCl溶液,则会使电动势增高。( )
)︱Ag(+)中,若向银半电池中加入适量的NaCl溶液,则会使电动势增高。( )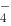 + 5Fe
+ 5Fe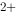 + 8H
+ 8H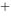 = Mn
= Mn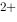 + 5Fe
+ 5Fe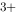 + 4H
+ 4H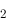 O 和 2Fe
O 和 2Fe + Sn
+ Sn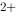 = 2Fe
= 2Fe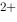 + Sn
+ Sn 均可自发进行,则下列标准电极电势最小的是( )。
均可自发进行,则下列标准电极电势最小的是( )。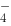 / Mn
/ Mn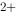 )
) (Fe
(Fe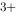 / Fe
/ Fe )
)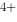 )
)




























