 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在相同温度下2H2(g)+S2(g)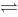 2H2S(g) Kp1 2Br2(g)+2H2S(g)
2H2S(g) Kp1 2Br2(g)+2H2S(g) 4HBr(g)+S2(g) Kp2 H2(g)+Br2(g)
4HBr(g)+S2(g) Kp2 H2(g)+Br2(g) 2HBr(g) Kp3 则Kp2等于
2HBr(g) Kp3 则Kp2等于
A.Kp1´Kp3
B.(Kp3)2/Kp1
C.2´Kp1´Kp2
D.Kp2/Kp1
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 A,占比40%
- · 有4位网友选择 D,占比40%
- · 有1位网友选择 C,占比10%
- · 有1位网友选择 B,占比10%



 2HD(g)的平衡常数Kө=3.78,同温下反应HD
2HD(g)的平衡常数Kө=3.78,同温下反应HD ½H2+½D2的Kө为
½H2+½D2的Kө为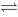 2H2S(g);Kp1 2Br2(g)+2H2S(g)
2H2S(g);Kp1 2Br2(g)+2H2S(g)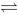 4HBr(g)+S2(g);Kp2 H2(g)+Br2(g)
4HBr(g)+S2(g);Kp2 H2(g)+Br2(g) 2HBr(g);Kp3 则Kp3等于
2HBr(g);Kp3 则Kp3等于 S32-(aq) Kc1=13.0 (2)S(s)+S22-(aq)
S32-(aq) Kc1=13.0 (2)S(s)+S22-(aq) S32-(aq) Kc2=10.8 (3)S(s)+S2-(aq)
S32-(aq) Kc2=10.8 (3)S(s)+S2-(aq) S22-(aq) Kc
S22-(aq) Kc
 N2O4(g), Kc/Kp等于
N2O4(g), Kc/Kp等于 =0.0404
=0.0404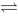 N2O4(g)平衡体系中NO2与N2O4分子数比为1:3,则气体平均相对分子质量为
N2O4(g)平衡体系中NO2与N2O4分子数比为1:3,则气体平均相对分子质量为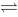 2T(g)的Kc=2.25,在平衡时T的浓度是3.00mol·dm-3,R的浓度是2.00mol·dm-3,则Q的浓度是
2T(g)的Kc=2.25,在平衡时T的浓度是3.00mol·dm-3,R的浓度是2.00mol·dm-3,则Q的浓度是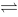 2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是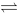 N2O4(g)达到平衡时,降低温度混合气体的颜色会变浅,说明此反应的逆反应是
N2O4(g)达到平衡时,降低温度混合气体的颜色会变浅,说明此反应的逆反应是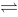 C,焓变小于零,若温度升高10℃,其结果是
C,焓变小于零,若温度升高10℃,其结果是 2CO2(g),ΔrHmө= -569 kJ·mol-1,提高CO的理论转化率的措施是
2CO2(g),ΔrHmө= -569 kJ·mol-1,提高CO的理论转化率的措施是




























