 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


关于实验室用二氧化锰与浓盐酸制备氯气的实验中,下列叙述正确的是()
A.浓盐酸具有还原性
B.浓硫酸用于除杂
C.氢氧化钠溶液用于吸收多余的氯气
D.氯气的密度比空气小
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A.浓盐酸具有还原性
B.浓硫酸用于除杂
C.氢氧化钠溶液用于吸收多余的氯气
D.氯气的密度比空气小
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“关于实验室用二氧化锰与浓盐酸制备氯气的实验中,下列叙述正确的是()”相关的问题
更多“关于实验室用二氧化锰与浓盐酸制备氯气的实验中,下列叙述正确的是()”相关的问题
用如图所示装置探究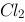 和
和 在
在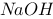 溶液中的反应,若通入适当比例的
溶液中的反应,若通入适当比例的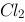 和
和 ,即发生反应
,即发生反应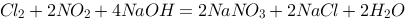 ,下列叙述正确的是
,下列叙述正确的是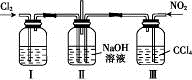
A、实验室中用二氧化锰与3mol/L的盐酸共热制备氯气
B、装置Ⅰ中盛放的试剂是浓硫酸,作用是干燥氯气
C、装置Ⅲ的作用是便于控制通入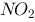 的量
的量
D、若制备的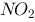 中含有
中含有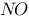 ,应将混合气体通入水中以除去
,应将混合气体通入水中以除去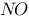
| 我们已经学过氢气、氧气、二氧化碳、氯气、二氧化硫、氨气等气体的制备方法和化学性质.以下是实验室制备、洗涤、干燥气体及进行尾气处理的常见仪器装置.请结合所学知识回答下列问题:
(1)下列气体中,只能用碱石灰干燥的是______(填字母). A.H2B.Cl2C.SO2D.NH3E.O2 (2)实验室用软锰矿(主要成分是MnO2)与浓盐酸混合加热制得氯气,所选制备装置是______,干燥氯气的装置是______,尾气处理装置是______. (3)实验室用氯化铵和熟石灰制取氨气,其化学反应方程式为______,收集氨气的方法是______,检验收集氨气已满的常用方法是______(任写一种). |
A、大量NaClO溶液中通入少量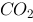 ,密封,置于阳光下
,密封,置于阳光下
B、向100mL18.4mol/L的浓硫酸中加入64g铜
C、标准状况下,将lg铝片投入20mL 18.4mol/L的浓硫酸中
D、用50mL 8mol/L浓盐酸与10g二氧化锰共热制取氯气
实验室中,常用盐酸与二氧化锰作用制取氯气,如何控制条件使反应MnO2+4HCl→Cl2+MnCl2+2H2O正向进行?为什么?当其他物质均处于标准态时,若反应正向进行,HCl的最低浓度为多大?
下列实验设计及其对应的离子方程式均正确的是()。
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+
B.Na202与H20反应制备02:Na2O2+H2O======2Na++2OH+O2↑
C.将氯气溶于水制备次氯酸:Cl2+H2O=====2H++C1+ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H202具有还原性:2MnO4-+6H++5H202====2Mn2++5O2↑+8H2O

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
