 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


已知电极电位:E0CU2+/CU=0.34V,E0Fe2+/Fe=- 0.44V,E0Fe3+/Fe=-0.04V,E0Fe3+/Fe2+=0.77V,将铁片放入CuSO4溶液中,铁变成什么离子?()
A.Fe2+
B.Fe3+
C.不变化
D.Fe2+和Fe3+
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 C,占比40%
- · 有2位网友选择 B,占比20%
- · 有2位网友选择 D,占比20%
- · 有2位网友选择 A,占比20%



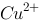 +2
+2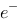 = Cu的平衡电极电位高于2
= Cu的平衡电极电位高于2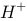 + 2
+ 2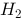 的平衡电极电位,所以()
的平衡电极电位,所以()





























