 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友LB4260851
发布时间:2022-01-07
[主观题]
BCl3在水中能发生水解的原因是中心原子B具有空的p轨道可以接受水中OH上的孤对电子。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“BCl3在水中能发生水解的原因是中心原子B具有空的p轨道可以接受水中OH上的孤对电子。”相关的问题
更多“BCl3在水中能发生水解的原因是中心原子B具有空的p轨道可以接受水中OH上的孤对电子。”相关的问题
推导结构
写出下列物质的中心原子杂化轨道类型,并画出其几何构型(包括孤对电子)。
BeCl2BCl3NH4+SF4BrF3
指出下列分子中,中心原子的杂化轨道类型和分子的空问构型。
CCl4、H2O、BCl3、BeCl2、NH3。
CH2F2和BCl3分子中的中心原子的轨道杂化类型分别为______,分子的形状分别为______;______为极性分子,______为非极性分子。
下列分子或离子中,中心原子的杂化轨道与NH3分子的中心原子杂化轨道最相似的是
(A) H2O; (B) H3O+; (C)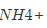 ; (D) BCl3。
; (D) BCl3。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
