 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
浓度为0.10 mol/L的HAc(pKa=4.74)溶液的pH等于_____ 。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“浓度为0.10 mol/L的HAc(pKa=4.74)溶液的pH等于_____ 。”相关的问题
更多“浓度为0.10 mol/L的HAc(pKa=4.74)溶液的pH等于_____ 。”相关的问题
浓度为0.1mol/L的某弱酸弱碱盐NH4A溶液pH=7.00,则HA的pKa为( )(已知:NH3·H2O的Kb=1.8×10-5)。
A.9.26 B.4.47 C.7.00 D.10.00
以0.020mol·L-1EDTA滴定浓度均为0.020mol·L-1Pb2+和Ca2+混合溶液中的Pb2+,终点时pH=5.0的HAc-Ac-缓冲溶液,c(Ac-)为0.1mol·L-1。若以二甲酚橙为指示剂,计算化学计量点时的pPb'sp、pCaY和终点误差。(lgKPbY=18.04,lgKCaY=10.7;pH=5.0时,lgαY(H)=6.45,pPbep(XO)=7.0;Pb2+-Ac-络合物的lgβ1和lgβ2分别为1.9、3.3,HAc的pKa=4.74)
已知:pKayΘ(HCOOH)=3.75,pKayΘ(HAc)=4.75,p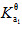 (H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
(H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?

 .计算此溶液的pH值以及[Ac-][PO43-]的浓度各为多少?H3PO4的pKa1~pKa2分别为2.12、7.20、12.36,HAc的pKa=4.74.
.计算此溶液的pH值以及[Ac-][PO43-]的浓度各为多少?H3PO4的pKa1~pKa2分别为2.12、7.20、12.36,HAc的pKa=4.74.
含0.10mol·L-1HCt和1.0mol·L-1HAc(pKa=4.74)的混合溶液的pH值为( )
(A) 2.37。 (B) 1.30。 (C) 1.00。 (D) 3.37。
A、64 ml、36 ml
B、50 ml、50 ml
C、36 ml、64 ml
D、28 ml、72 ml

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
