 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,电池反应Ag + 1/2Hg2Cl2 = AgCl + Hg的电池电动势为0.0193V,反应所对应的△S为32.9J/K,则该电池电动势的温度系数为
A.1.7×10-4V/k
B.1.1×10-6V/k
C.1.01×10-1V/k
D.3.4×10-4V/k
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 D,占比40%
- · 有3位网友选择 C,占比30%
- · 有2位网友选择 A,占比20%
- · 有1位网友选择 B,占比10%



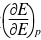 为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。




























