 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
H2(g)+Cl2(g)=2HCl(g)反应机理是: Cl2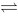 2Cl (快) Cl+H2=HCl+H (慢) 则该反应的速率方程是
2Cl (快) Cl+H2=HCl+H (慢) 则该反应的速率方程是
A.v=kc(H2)·c(Cl2)
B.v=kc(Cl2)½·c(H2)
C.v=kc(H2)·c(Cl)
D.v=kc(Cl2)2·c(H2)
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有6位网友选择 B,占比66.67%
- · 有2位网友选择 C,占比22.22%
- · 有1位网友选择 A,占比11.11%



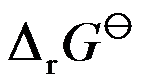 和
和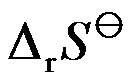 分别为
分别为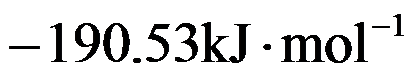 和
和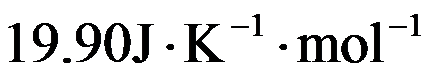 ,则HCl(g)的标准摩尔生成焓为( )。
,则HCl(g)的标准摩尔生成焓为( )。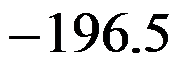
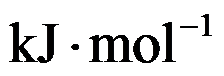
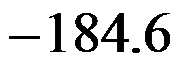
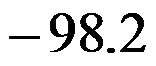
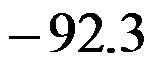
 CH3COCH2Br(aq)+HBr(aq) 此反应对于溴来说是零级,下述推断正确的是
CH3COCH2Br(aq)+HBr(aq) 此反应对于溴来说是零级,下述推断正确的是
 3C正逆反应的活化能分别为m kJ·mol-1和n kJ·mol-1,则反应的ΔrHm/kJ·mol-1为
3C正逆反应的活化能分别为m kJ·mol-1和n kJ·mol-1,则反应的ΔrHm/kJ·mol-1为 HCOOH +CH3OH v = k (HCOOCH3) (H+) 在反应方程式中没有H+,而速率方程中有(H+),对此的解释是
HCOOH +CH3OH v = k (HCOOCH3) (H+) 在反应方程式中没有H+,而速率方程中有(H+),对此的解释是
 H2,此反应的活化能为
H2,此反应的活化能为




























