 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定温度下,反应PCl3(g)+Cl2(g)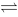 PCl5(g)达到平衡,当进行下列操作时,平衡不发生变化的是
PCl5(g)达到平衡,当进行下列操作时,平衡不发生变化的是
A.在恒容条件下,通入一定量的水蒸气
B.在恒容条件下,通入一定量的氮气
C.在恒压条件下,通入一定量的氮气
D.在恒压条件下,通入一定量的水蒸气
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有3位网友选择 B,占比30%
- · 有3位网友选择 C,占比30%
- · 有3位网友选择 A,占比30%
- · 有1位网友选择 D,占比10%



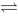 PCl3(g)+Cl2(g)在密闭容器中进行,其焓变小于零。当达到平衡时,下列说法正确的是
PCl3(g)+Cl2(g)在密闭容器中进行,其焓变小于零。当达到平衡时,下列说法正确的是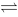 NH3(g)+H2S(g),若通过下述各措施,反应再达平衡时,NH3的分压比原平衡态的分压减小的措施是
NH3(g)+H2S(g),若通过下述各措施,反应再达平衡时,NH3的分压比原平衡态的分压减小的措施是
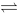 2SO3(g),达到平衡,加一定量N2气体保持总压力不变,平衡将会
2SO3(g),达到平衡,加一定量N2气体保持总压力不变,平衡将会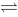 2NH3(g),反应达到平衡后,把PNH3,PH2各提高到原来的2倍,PN2不变,则平衡将会
2NH3(g),反应达到平衡后,把PNH3,PH2各提高到原来的2倍,PN2不变,则平衡将会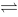 CO2(g)+H2(g) ΔrHmө = -41.2kJ·mol-1,为提高CO转化率可采用
CO2(g)+H2(g) ΔrHmө = -41.2kJ·mol-1,为提高CO转化率可采用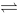 2HBr(g)的Kc=1.86。若将3mol H2,4mol Br2和5mol HBr放在10 dm3烧瓶中,则
2HBr(g)的Kc=1.86。若将3mol H2,4mol Br2和5mol HBr放在10 dm3烧瓶中,则




























