 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...
已知H2A的Ka1= 1×10![已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...已知H2](https://img2.soutiyun.com/shangxueba/ask/19308001-19311000/19308509/c7d026b-chaoxing2016-151644.jpeg) , Ka2= 1×10
, Ka2= 1×10![已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...已知H2](https://img2.soutiyun.com/shangxueba/ask/19308001-19311000/19308509/9fec39e-chaoxing2016-151653.jpeg) , 现将0.1mol的NaHA配成1L溶液,其pH= _____________
, 现将0.1mol的NaHA配成1L溶液,其pH= _____________
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知H2A的Ka1= 1×10![已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...已知H2](https://img2.soutiyun.com/shangxueba/ask/19308001-19311000/19308509/c7d026b-chaoxing2016-151644.jpeg) , Ka2= 1×10
, Ka2= 1×10![已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...已知H2](https://img2.soutiyun.com/shangxueba/ask/19308001-19311000/19308509/9fec39e-chaoxing2016-151653.jpeg) , 现将0.1mol的NaHA配成1L溶液,其pH= _____________
, 现将0.1mol的NaHA配成1L溶液,其pH= _____________
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……
 更多“已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...”相关的问题
更多“已知H2A的Ka1= 1×10 [图], Ka2= 1×10 [图], 现...”相关的问题
已知H2A的Ka1= 1×10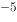 , Ka2= 1×10
, Ka2= 1×10 , 现将0.1mol的NaHA配成1L溶液,其pH= _____________
, 现将0.1mol的NaHA配成1L溶液,其pH= _____________
已知H2A的Ka1= 1×10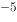 , Ka2= 1×10
, Ka2= 1×10 , 现将0.1mol的NaHA配成1L溶液,其pH= _____________
, 现将0.1mol的NaHA配成1L溶液,其pH= _____________
已知某二元酸H2A的一级电离是完全的,二级电离不完全。若0.010mol·dm-3的H2A溶液的pH=1.84,求该酸的第二级解离常数。
已知H2A的Ka2Θ为10—7,Ka2Θ为1013,则0.1mol.L—1H2A水溶液的pH为()。
A.13
B.2
C.3
D.4
| 某二元弱酸(简写成H2A)溶液,按下式发生一级和二级电离:H2A?H++HA-,HA-?H++A2-,已知同浓度时电离程度H2A远大于HA-.设有下列四种溶液: ①0.01mol/LH2A溶液 ②0.01mol/LNaHA溶液中 ③0.02mol/LHCl与0.04mol/LNaHA等体积混合 ④0.02mol/LNaOH与0.02mol/LNaHA等体积混合 (1)写出溶液③中HCl和NaHA反应的离子方程式______; (2)四种溶液中c(H+)从大到小的顺序是______; (3)四种溶液中c(A2-)最大的是______,最小的是______. |
A.2.0×10-9
B.2.4×10-13
C.1.2×10-4
D.2.6×10-6
E.1.4×10-5
| 已知H2A为弱酸,下列说法错误的是 A.0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+ c(H2A)= 0.1mol/L B.常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 C.常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 D.常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9 |

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
