 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用间接碘量法测定铜时,Fe3+和AsO43-都能氧化I-而干扰铜的测定,加入0.005 mol.dm-3NH4HF2即能消除
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“用间接碘量法测定铜时,Fe3+和AsO43-都能氧化I-而干扰铜的测定,加入0.005 mol.dm-3NH4HF2即能消除”相关的问题
更多“用间接碘量法测定铜时,Fe3+和AsO43-都能氧化I-而干扰铜的测定,加入0.005 mol.dm-3NH4HF2即能消除”相关的问题
用间接碘量法测定铜时,Fe3+和[AsO4]3-都能氧化I-而干扰铜的测定,加入0.005mol•L-1NH4HF2即能消除Fe3+及[AsO4]3-的干扰。试以计算说明之。已知
![用间接碘量法测定铜时,Fe3+和[AsO4]3-都能氧化I-而干扰铜的测定,加入0.005mol•L](https://img2.soutiyun.com/ask/2020-06-03/960053042727707.png)
![用间接碘量法测定铜时,Fe3+和[AsO4]3-都能氧化I-而干扰铜的测定,加入0.005mol•L](https://img2.soutiyun.com/ask/2020-06-03/960053093646196.png)
HF的Ka=7.4x10-4;[FeF6]2-的lgβ1~lgβ3的值为5.3、9.3、12.0。(提示:HF-F-缓冲体系[H+]计算不能用最简式。)
间接碘量法测定铜时Fe3+和AsO4都能氧化I-而干扰铜的测定,加入0.005mol.L-1NH4HF2即
能除Fe3+及AsO4的干扰。试以计算说明之。
(EAs(v)/As(III)=0.229V EFe3+/Fe2+=0.771V EIΘΘΘ23-/I-=0334V HF的
2-Ka=7.4×10-4 FeF6的lgβ1-lgβ3为 5.3 9.3 12.0)
(提示HF-F-缓冲体系[H+]计算不能用最简式,EAs(V)/As(III)=0.368<EI2/I- Θ'
EFe3+/Fe2+Θ=0.460<EI2/I-Θ`Θ)
+CHF-[H+]-3.130.005-[H]
用间接碘量法测定铜时,Fe3+和AsO43-都能氧化I-而干扰铜的测定,加入
0.005molL-1NH4HF2即能消除Fe3+和AsO43-的干扰.试以计算说明之.(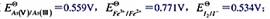 HF的
HF的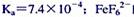 的lgβ1~lgβ3的值为5.3,9.3,12.0)
的lgβ1~lgβ3的值为5.3,9.3,12.0)
(HF-F-缓冲体系([H+]计算不能用最简式.)
解释下列现象:
a.将氯水慢慢加入到含有Br-和I-的酸性溶液中,以CCl4萃取,CCl4层变为紫色;
b.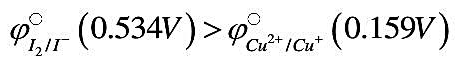 ,但是Cu2+却能将I-氧化为I2;
,但是Cu2+却能将I-氧化为I2;
c.间接碘量法测定铜时,Fe3+和[AsO4]3-都能氧化I-析出I2,因而干扰铜的测定,加入NH4HF2两者的干扰均可消除;
d.Fe2+的存在加速KMnO4氧化Cl-的反应:
e.以KMnO4滴定[C2O4]2-时,滴入KMnO4的红色消失速度由慢到快。
f.于K2Cr2O7标准溶液中,加入过量KI,以淀粉为指示剂,用Na2S2O3溶液滴定至终点时,溶液由蓝变为绿;
g.以纯铜标定Na2S2O3溶液时,滴定到达终点后(蓝色消失)溶液又返回到蓝色。
参考答案:
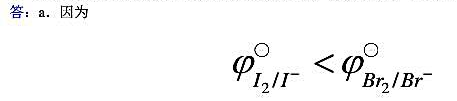

7、增加溶液的离子强度,Fe3+/Fe2+电对的条件电势是升高还是降低?加入[PO4]3-,F-或1,10-邻二氮菲后,情况又如何?
)间接碘量法测定铜时,若试液中有Fe3+;AsO43-,它们都可将碘离子氧化成碘单质,加入NH4HF2可消除两者的干扰,解释其中原因。
用间接碘量法测定制时,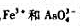 都能氧化I+而干扰铜的测定,加入0.005mol·L-1NH4HF2即能消除
都能氧化I+而干扰铜的测定,加入0.005mol·L-1NH4HF2即能消除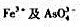 的干扰。试以计算说明之。
的干扰。试以计算说明之。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
