 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
判断298K,标准状态下,MnO2能否氧化盐酸制取氯气?若用浓盐酸(12 molL-1)与MnO2作用[设c(Mn2+)=1.0
判断298K,标准状态下,MnO2能否氧化盐酸制取氯气?若用浓盐酸(12 molL-1)与MnO2作用[设c(Mn2+)=1.0molL-1,,J(Cl2)=100kPa],能否制得氯气?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
判断298K,标准状态下,MnO2能否氧化盐酸制取氯气?若用浓盐酸(12 molL-1)与MnO2作用[设c(Mn2+)=1.0molL-1,,J(Cl2)=100kPa],能否制得氯气?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“判断298K,标准状态下,MnO2能否氧化盐酸制取氯气?若用浓盐酸(12 molL-1)与MnO2作用[设c(Mn2+)=1.0”相关的问题
更多“判断298K,标准状态下,MnO2能否氧化盐酸制取氯气?若用浓盐酸(12 molL-1)与MnO2作用[设c(Mn2+)=1.0”相关的问题
由二氧化锰制备金属锰可采取下列两种方法: (1)MnO2(S)+2H2(g)=Mn(S)+2H2O(g) △rHΘm=37.22kJmol-1 △rSΘm=94.96Jmol-1K-1 (2)MnO2(s)+2C(s)=Mn(S)+2CO(g) △rHΘm=299.8kJmol-1 △rSΘm=363.3Jmol-1K-1 试通过计算确定上述两个反应在298K、标准态下的反应方向。如果考虑工作温度越低越好,则采用哪种方法较好? 解题思路:①标准状态下298K时的反应方向,应由△rGΘm(298.K)判断。 ②工作温度则应根据转化温度来确定。
利用298.15K时有关电对的标准电极电势,试回答下列问题:
(1)在298.15K、标准状态下,I2能否将Mn2+氧化为MnO2?
(2)在298.15K、标准状态下,KMnO4在酸性溶液中能否将Fe2+氧化为Fe2+?
(3)在298.15K、标准状态下,Sn2+能否将Fe3+还原为Fe2+?
(4)在298.15K、标准状态下,Sn2+能杏将Fe2+还原为Fe?
(1)计算298K下反应: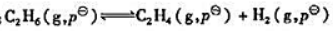 的
的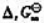 并判断在标准状态下反应向何方进行.
并判断在标准状态下反应向何方进行.
(2)计算298K反应: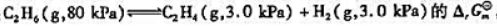 并判断反应方向.
并判断反应方向.
计算298K时,反应 Sn2+(aq)+Pb(s)=Sn(s)+pb2+(aq)的△rGΘm,并判断标准状态下反应的自发方向。
A.平衡状态
B.正向
C.逆向
D.无法判断
A.在标准状态下, 298K 时反应能自发进行
B.在标准状态下, 298K 时反应不能自发进行
C.该反应是吸热反应
D.该反应是熵减反应

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
