 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友18***469
发布时间:2022-01-07
[主观题]
下列叙述是否正确?并加以解释。 (1)所有化学反应的反应速率都随时间的变化而发生改变; (2)可以从速率系数的单位来推测反应级数和反应分子数: (3)正反应的活化能一定大于逆反应的活化能: (4)按过渡状态理论,正反应和逆反应应具有相同的活化配合物。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
查看官方参考答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“下列叙述是否正确?并加以解释。 (1)所有化学反应的反应速率都随时间的变化而发生改变; (2)可以从速率系数的单位来推测反应级数和反应分子数: (3)正反应的活化能一定大于逆反应的活化能: (4)按过…”相关的问题
更多“下列叙述是否正确?并加以解释。 (1)所有化学反应的反应速率都随时间的变化而发生改变; (2)可以从速率系数的单位来推测反应级数和反应分子数: (3)正反应的活化能一定大于逆反应的活化能: (4)按过…”相关的问题
A、各物质的浓度或分压不随时间而变化
B、
C、改变化学平衡体系压力,必定会导致平衡发生移动,直至达到新的平衡
D、如果寻找到该反应的高效催化剂,可提高其平衡转化率
基态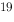 K原子最外层电子的四个量子数表达正确的有:
K原子最外层电子的四个量子数表达正确的有:
A、(4,1,0,+1/2)
B、(4,1,1,+1/2)
C、(3,0,0,+1/2)
D、(4,0,0,+1/2)
反应A(g)+2B(s)=3Z(g),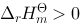 当反应在一定温度下达到化学平衡后,下列说法正确的是:
当反应在一定温度下达到化学平衡后,下列说法正确的是:
A、升高温度可以使化学平衡正向移动
B、将反应容器的体积压缩不能使平衡发生移动
C、充入惰性气体可以使化学平衡正向移动
D、加入催化剂可以使化学平衡正向移动
某基元反应热效应△rH =50 kJ·mol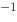 ,则该反应的活化能Ea为:
,则该反应的活化能Ea为:
A、≥50 kJ/mol
B、<50 kj> C、-50 kJ/mol
D、无法确定

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
