 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
630K时, (1)计算该反应在630K时的标准平衡常数; (2)将A(s)放入一真空容器内,在630K达到化
630K时,
(1)计算该反应在630K时的标准平衡常数;
(2)将A(s)放入一真空容器内,在630K达到化学平衡时Y(g)和Z(g)的分压分别为多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
630K时,
(1)计算该反应在630K时的标准平衡常数;
(2)将A(s)放入一真空容器内,在630K达到化学平衡时Y(g)和Z(g)的分压分别为多少?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“630K时, (1)计算该反应在630K时的标准平衡常数; (2)将A(s)放入一真空容器内,在630K达到化”相关的问题
更多“630K时, (1)计算该反应在630K时的标准平衡常数; (2)将A(s)放入一真空容器内,在630K达到化”相关的问题
A、K1+K2
B、K1-K2
C、K1?K2
D、K1/K2
在 21.8℃ 时, 反 应 NH4HS (s)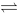 NH3 (g) + H2S (g) 的 标 准 平 衡 常 数 K= 0.070, 平 衡 混 合 气 体 总 压 是
NH3 (g) + H2S (g) 的 标 准 平 衡 常 数 K= 0.070, 平 衡 混 合 气 体 总 压 是
A、7.0 kPa
B、26 kPa
C、53 kPa
D、0.26 kPa
已知在一定温度下 SnO2(s) + 2H2(g) Sn(s) + 2H2O(g) K1θ= 21.0 CO(g) + H2O(g)
Sn(s) + 2H2O(g) K1θ= 21.0 CO(g) + H2O(g) CO2(g) + H2(g) K2θ= 0.0340 因此下列反应SnO2(s) + 2CO(g)
CO2(g) + H2(g) K2θ= 0.0340 因此下列反应SnO2(s) + 2CO(g) Sn(s) + 2CO2(g) 的K3θ值为
Sn(s) + 2CO2(g) 的K3θ值为
A、21.0
B、0.714
C、0.0243
D、21.1
B.c,d,a,b,e
C.c,e,a,b,d
D.d,b,a,e,c

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
