 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


已知常压下,20℃时,CO2在水中的亨利系数为1.44×105kPa,并且已知以下两个反应的平衡常数 若平衡状态下气
已知常压下,20℃时,CO2在水中的亨利系数为1.44×105kPa,并且已知以下两个反应的平衡常数
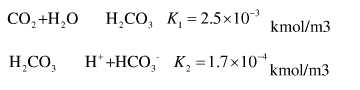
若平衡状态下气相中的CO2分压为10kPa,求水中溶解的CO2的浓度。
(CO2在水中的一级解离常数为K=4.3×10-7kmol/m3,实际上包含了上述两个反应平衡,K=K1K2)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)

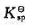 =2.8x10^-9,H2CO3的K1=4.5x10^-7,K2=4.7x10^-11。
=2.8x10^-9,H2CO3的K1=4.5x10^-7,K2=4.7x10^-11。 =2.8×10-9,H2CO3 的
=2.8×10-9,H2CO3 的
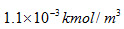 的25水溶液接触,试判断传质过程方向。
的25水溶液接触,试判断传质过程方向。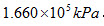 。
。





























