 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


298K时,测得电池 Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l) 的电动势为0.9265V,已知水的标准生成热=-285.81kJ
298K时,测得电池
Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l)
的电动势为0.9265V,已知水的标准生成热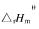 =-285.81kJ/mol,有关物质的规定熵数据如下:
=-285.81kJ/mol,有关物质的规定熵数据如下:

试求HgO在此温度下的分解压。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)


 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


298K时,测得电池
Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l)
的电动势为0.9265V,已知水的标准生成热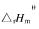 =-285.81kJ/mol,有关物质的规定熵数据如下:
=-285.81kJ/mol,有关物质的规定熵数据如下:

试求HgO在此温度下的分解压。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)


 更多“298K时,测得电池 Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l) 的电动势为0.9265V,已知水的标准生成热=-285.81kJ”相关的问题
更多“298K时,测得电池 Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l) 的电动势为0.9265V,已知水的标准生成热=-285.81kJ”相关的问题
298K时,测得电池Pt|H2(100kPa)|H2SO4(0.5mol/kg)|Hg2SO4(s)|Hg(l)的电动势为0.6960V,求H2SO4在溶液中的离子平均活度系数。已知
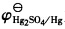 为0.6158V。
为0.6158V。
298K时,测得电池 Pt|H2(100kPa)|NaOH(aq)|HgO(s)|Hg(l) 的电动势为0.9265V,已知水的标准生成热△rHmΘ=一285.81kJ/mol,有关物质的规定熵数据如下: 物质 HgO(s) O2(g) H2O(1) Hg(1) H2(g) SmΘ/[J/(K.mol)] 72.22 205.10 70.08 77.40 130.67 试求HgO在此温度下的分解压。
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
298K时,已知如下电池的标准电动势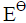 =0.2680V:
=0.2680V:
Pt|H2(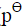 )|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)
)|HCl(0.08mol·kg-1, γ±=0.809)|Hg2Cl2(s)|Hg(l)

A.Pt,H2|OH-||H+|H2,Pt
B.Pt,H2|H+||OH-|H2,Pt
C.Pt,O2|H+||OH-|O2,Pt
D.Pt,H2|H+||OH-|O2,Pt
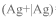 =0.799V,电池Pt|H2|H2SO4(aq)|Ag2SO4(s)|Ag(s)为0.627V,Ag2SO4的活度积为( )
=0.799V,电池Pt|H2|H2SO4(aq)|Ag2SO4(s)|Ag(s)为0.627V,Ag2SO4的活度积为( )
A.3.8×10-17
B.1.2×10-3
C.2.98×10-3
D.1.52×10-6
298K时,电池Pt|H2(100kPa)|HCl(m)|Hg2Cl2(s)|Hg(l)在不同盐酸浓度时的电动势数值为
 试用作图法求出该电池的标准电动势,并计算盐酸浓度为0.07508mol/kg时的离子平均活度系数。
试用作图法求出该电池的标准电动势,并计算盐酸浓度为0.07508mol/kg时的离子平均活度系数。
请:
(1)写出电极反应和电池反应;
(2)求正极Cl-(0.1mol·kg-1,γ±=0.798)|AgCl(s)IAg(s)的标准电极电势:
(3)求电池反应H2(g)+2AgCl(s)→2Ag(s)+2HCl的标准平衡常数.
已知298K时下述电池的电动势为1.362V,
(Pt)H2(pθ)|H2SO4(aq)|Au2O3=Au(s)
又知H2O(g)的ΔrGmθ=-228.6kJ·mol-1,该温度下水的饱和蒸汽压为3167Pa,
求在298K时氧气的逸度为多少才能使Au2O3与Au呈平衡?
计算298K时下述电池的电动势E。
Pb(s)|PbCl2(s)|HCl(0.01mol·kg-1)|H2(10kPa)|Pt
已知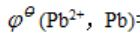 =-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。
=-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
