 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用教材附表中的数据,计算298K下反应:的标准平衡常数.
用教材附表中的数据,计算298K下反应: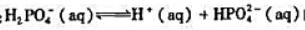 的标准平衡常数.
的标准平衡常数.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用教材附表中的数据,计算298K下反应: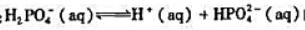 的标准平衡常数.
的标准平衡常数.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“用教材附表中的数据,计算298K下反应:的标准平衡常数.”相关的问题
更多“用教材附表中的数据,计算298K下反应:的标准平衡常数.”相关的问题
(1)由附表六中查出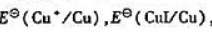 试计算
试计算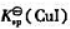 .
.
(2)计算298K下反应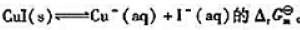
(3)若已知(2)中反应的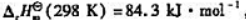 计算该反应的
计算该反应的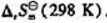
根据教材附表一中的相关数据主考虑电势图N2-HN4+,(aq)-NH;(aq)在酸性溶液中Eθ(N2/HN3)和Eθ(HN3/NH4+).写出HN3(aq)的岐化反应方程,计算25℃下该反应的标准平衡常数Kθ并评价NH3(aq)的稳定性.
已知反应:
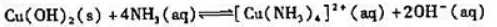
(1)计算该反应在298K下的标准平衡常数;
(2)估算Cu(OH)2在6.0mol·L-1氨水中的溶解度(mol·L-1)(忽略氨水浓度的变化).
已知反应:

298K时的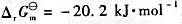 。试计算:
。试计算:
(1)该反应的标准平衡常数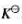 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。
将N2气缓慢通过高温调粉可以发生如下的反应: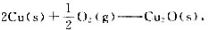 .
.
请计算:
(1)298K下该反应的标准平衡常数;
(2)若600℃下,让总压为200kPa的含氧的氮气缓慢通过铜粉(可认为反应达到平衡),纯化后的氮气中残留氧的分压和体积百分数.

298K时,已知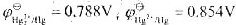 ,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。
,试计算(1)反应Hg2++e→1/2Hg22+的标准电极电势。(2)为反应Hg+Hg2+→Hg2-设计电池,并计算该反应的标准平衡常数。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
