 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


室温时,0.01mol/L某一元弱酸HA中,有1%的HA发生了电离,则下列说法正确的是()
A.上述弱酸溶液的pH=2
B.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH=7
C.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH>7
D.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH<7
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A.上述弱酸溶液的pH=2
B.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH=7
C.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH>7
D.加入等体积的0.01mol/LNaOH溶液后,所得溶液的pH<7
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“室温时,0.01mol/L某一元弱酸HA中,有1%的HA发生了电离,则下列说法正确的是()”相关的问题
更多“室温时,0.01mol/L某一元弱酸HA中,有1%的HA发生了电离,则下列说法正确的是()”相关的问题
已知某一元弱酸的浓度为0.01mol/L,pH=4.55,则其解离常数Ka为()。
A.5.8×10-2
B.9.8×10-3
C.8.6×10-7
D.7.97×10-8
已知某一元弱酸的浓度为0.01mol/L,pH=4.55,则其解离常数Ka为()。
A.5.8×l0-2
B.9.8×l0-3
C.8.6×10-7
D.7.97×10-8
A.中性红(6.8-8.0)
B.酚酞(8.3-10.0)
C.甲基橙(3.1-4.4)
D.甲基红(4.0-6.2)
某一元弱酸(HA)纯品1.250g,用水溶解后定容至50.00mL,用41.20mL0.0900mol·L-1NaOH标准溶液滴定至化学计量点。加入8.24mL NaOH溶液时,溶液pH为4.30。求:
(1)弱酸的摩尔质量
(2)弱酸的解离常数
(3)化学计量点的pH
(4)选用何种指示剂
某一元弱酸HA溶液的[H+]=amol•dm-3,在此溶液中加入过量难溶盐MA,实现沉淀溶解平衡时,溶液的[H+]=bmol•dm-3。设酸的浓度满足解离平衡的近似计算条件,求MA的溶度积常数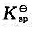 。
。
某一弱酸(HA)1.250g,用水溶解后稀释至50.00mL,可用41.20mL0.09000mol/L的标准氢氧化钠溶液滴定至化学计量点。当加入NaOH溶液8.24mL时,该溶液的pH为4.30,求(1)求该弱酸的摩尔质量和解离常数Ka及计量点的PH(2)选择何种指示剂?
平衡时,溶液的c(H+)=b mol·dm-3设酸的浓度满足解离平衡的近似计算条件,试求MA的溶度积常数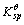 。
。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
