 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
10. 已知SO2(g)和O2(g)的标准热力学函数数据如下: 物质 SO2(g) SO3(g) O2(g) DfHmy(298.15K) / kJ·mol-1 -296.9 -359.2 0 Sm y(298.15K) / J· mol-1·K-1 248.1 256.23 205.03 利用上述数据,求反应: SO2(g) + O2 = SO3(g) 在25℃时的DrGm y及 K y 。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……

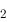 CO
CO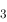 (s)= Ag
(s)= Ag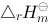 /kJ·mol
/kJ·mol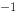 -505.8 -31.1 -393.5 标准状态下, 该反应的恒压反应热 kJ·mol
-505.8 -31.1 -393.5 标准状态下, 该反应的恒压反应热 kJ·mol 分别为 -50.8, -394.4, -237.2 kJ·mol-1,则 298 K时 ,CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O(l) 的
分别为 -50.8, -394.4, -237.2 kJ·mol-1,则 298 K时 ,CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O(l) 的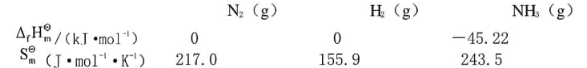 在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。
在该温度下反应N2+3H2(g)====2NH3(g)达平衡时,[N2]=1.0mol·dm-3,[H2]=3.0mol·dm-3。求NH3的浓度。




























