 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)将反应H2(pθ)+I2(s)=2HI(a=1)设计成电池;(2)求此电池的Eθ及电池反应2
(1)将反应H2(pθ)+I2(s)=2HI(a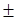 =1)设计成电池;(2)求此电池的Eθ及电池反应25℃时的Kθ;(3)若反应写成
=1)设计成电池;(2)求此电池的Eθ及电池反应25℃时的Kθ;(3)若反应写成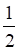 H2(pθ)+ I2(s)=HI(a
H2(pθ)+ I2(s)=HI(a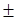 =1),电池的Eθ及反应的Kθ之值与.(2)相同否?为什么?
=1),电池的Eθ及反应的Kθ之值与.(2)相同否?为什么?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(1)将反应H2(pθ)+I2(s)=2HI(a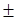 =1)设计成电池;(2)求此电池的Eθ及电池反应25℃时的Kθ;(3)若反应写成
=1)设计成电池;(2)求此电池的Eθ及电池反应25℃时的Kθ;(3)若反应写成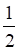 H2(pθ)+ I2(s)=HI(a
H2(pθ)+ I2(s)=HI(a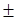 =1),电池的Eθ及反应的Kθ之值与.(2)相同否?为什么?
=1),电池的Eθ及反应的Kθ之值与.(2)相同否?为什么?
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“(1)将反应H2(pθ)+I2(s)=2HI(a=1)设计成电池;(2)求此电池的Eθ及电池反应2”相关的问题
更多“(1)将反应H2(pθ)+I2(s)=2HI(a=1)设计成电池;(2)求此电池的Eθ及电池反应2”相关的问题
将反应2Cu(s)+HgO(s)→Hg(l)+Cu2O(s)设计成电池时,其电池表示为______。
将下列反应设计成原电池,并应用教材中表7.7.1的数据计算25℃时电池反应的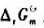 及
及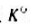 .
.
(1)2Ag++H2(g)=2Ag+2H+
(2)Cd+Cu2+=Cd2++Cu
(3)Sn2++Pb2+=Sn4++Pb
(4)2Cu+=Cu+Cu2+
将氧化还原反应2Mn04-+10C1-+16H+=2Mn2++5C12+8H20设计成原电池,该电池的符号为(7) 。
将下列两个反应设计成电池,此两电池的EΘ、△rGmΘ及Ka的关系为() ①Fe(s)+2Fe3+(a1)→3Fe2+(a2) ②2Fe(s)+4Fe3+(a1)→6Fe2+(a2)
A.EΘ(1)=EΘ(2),△rGmΘ(11)=△rGΘ(2),KaΘ(1)=KaΘ(2)
B.EΘ(1)=EΘ(2),△rGmΘ(2)=2△rGΘ(1),KaΘ(2)=[KaΘ(1)]2
C.EΘ(2)=EΘ(1),△rGmΘ(2)=2△rGΘ(1),KaΘ(2)=[KaΘ(1)]2
D.EΘ(1)=EΘ(2),△rGmΘ(2)=2△rGΘ(1),KaΘ(1)=KaΘ(2)
将反应Ag(s)→Ag-Au(合金,a(Ag)=0.1)设计成原电池图式为______,25℃时该电池的电动势E=______。
可以将反应Zn+Br2===ZnBr2设计成可充电电池,下列4个电极反应: ①Br2+2e-===2Br- ②2Br--2e-===Br2 ③Zn-2e-===可以将反应Zn+Br 2 ===ZnBr 2 设计成可充电电池,下列4个电极反应: ①Br 2 +2e - ===2Br - ②2Br - -2e - ===Br 2 ③Zn-2e - ===Zn 2+ ④Zn 2+ +2e - ===Zn 其中表示充电时的阳极反应和放电时的负极反应的分别是 [ ]②和③ B.②和① C.③和① D.④和①
A.②和③
B.②和①
C.③和①
D.④和①

A.由题目可知,反应(1)中出现了银离子,所以设计成电池一定会有银电极。
B.由题目可知,反应(1)中出现了银离子,所以设计成电池一定会有氯气体电极。
C.由题目可知,反应(2)中有很明显的氧化还原反应,氯得电子还原了,是电池的负极。
D.由题目可知,反应(2)中有很明显的氧化还原反应,碘离子失电子氧化了,是电池的正极。
试设计一个电池,使其中进行下述反应:

(1)写出电池表示式;
(2)计算25℃时,上述电池反应的Kθ;
(3)若将过量的银粉加到浓度为0.05mol·kg-1的Fe(NO3)3溶液中,求反应达平衡后Ag+的浓度为多少?(设活度系数均为1).已知φθ(Fe3+|Fe2+)=0.771V,φθ(Ag|Ag+)=0.7991V.
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
将Ag---AgCl电极[E(AgCl/Ag)=0.2222V]与饱和甘汞电极[E=0.2415v]组成原电池, 该原电池的电池符号为________________;正极反应________________;负极反应______________;电池反应___________________;电池的平衡常数为________________.

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
