 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
pH玻璃电极与饱和甘汞电极组成如下测量电池:298K时测得pH=5.00标准缓冲溶液的电池电动势为0.21
pH玻璃电极与饱和甘汞电极组成如下测量电池:

298K时测得pH=5.00标准缓冲溶液的电池电动势为0.218V。若用未知溶液代替标准缓冲溶液,测得两未知pH溶液的电池电动势分别为0.162V和0.252V,试计算这两个未知溶液的pH值。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
pH玻璃电极与饱和甘汞电极组成如下测量电池:

298K时测得pH=5.00标准缓冲溶液的电池电动势为0.218V。若用未知溶液代替标准缓冲溶液,测得两未知pH溶液的电池电动势分别为0.162V和0.252V,试计算这两个未知溶液的pH值。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“pH玻璃电极与饱和甘汞电极组成如下测量电池:298K时测得pH=5.00标准缓冲溶液的电池电动势为0.21”相关的问题
更多“pH玻璃电极与饱和甘汞电极组成如下测量电池:298K时测得pH=5.00标准缓冲溶液的电池电动势为0.21”相关的问题
pH玻璃电极与饱和甘汞电极组成如下电池:玻璃电极|H+(x)‖饱和甘汞电极。测定pH为4.01的邻苯二甲酸氢钾缓冲溶液时,其电池电动势为0.211V。而测定两个未知溶液时,其电池电动势分别为0.435V和0.0186V,试计算两种未知溶液的pH(25℃)。
298K时测定下述电池的电动势:
玻璃电极|pH缓冲溶液|饱和甘汞电极
当所用缓冲溶液的pH=4.00时,测得电池的电动势为0.1120V。若换用另一缓冲溶液重测电动势,得E=0.3865V。试求该缓冲溶液的pH值。当电池中换用pH=2.50的缓冲溶液时,计算电池的电动势E。
在25℃时用下列电池
标准氢电极|待测pH试液||饱和甘汞电极测得如下一系列溶液的电动势,试根据电动势计算溶液的pH。
下述电池的溶液为pH=4.00的标准缓冲溶液,25℃时测得电动势为0.209V:
pH玻璃电极|H+(a=x)‖饱和甘汞电极
当分别用三种未知溶液代替标准缓冲溶液时,测得电动势为:①0.312V;②0.088V;③-0.017V。试计算每种溶液的pH及氢离子活度。
以Ag/AgCl与玻璃电极组成如下电池:饱和玻璃电极

在25℃时。当标准缓冲溶液的pH=4.006,测得其中动势为-0.2094V。用一种未知pH的缓冲溶液代替上述已知pH的缓冲溶液,所测电动势值为-0.2806V,计算这种缓冲溶液的pH。
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
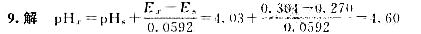
下列电池(25℃):
玻璃电极|标准溶液或未知液||饱和甘汞电极
当标准缓冲溶液的pH=4.00时电动势为0.209V,当缓冲溶液由未知溶液代替时,测得下到电动势值:①0.088V;②0.312V。求未知溶液的pH值。
A.玻璃电极和饱和甘汞电极;
B.玻璃电极和Ag—AgCl电极;
C.玻璃电极和标准甘汞电极;
D.饱和甘汞电极和Ag—AgCl电极。
A . 玻璃电极和Ag-AgCl电极
B . 玻璃电极和饱和甘汞电极
C . 玻璃电极和标准甘汞电极
D . 饱和甘汞电极和Ag-AgCl电极

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
