 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用下列电极反应在298K时的标准电极电势:Cu(OH)2+2e-→Cu+2OH- E1θ=-0
利用下列电极反应在298K时的标准电极电势:
Cu(OH)2+2e-→Cu+2OH- E1θ=-0.224V
Cu2++2e-→Cu E2θ=0.340V
求Cu(OH)2在298K时的活度积().
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用下列电极反应在298K时的标准电极电势:
Cu(OH)2+2e-→Cu+2OH- E1θ=-0.224V
Cu2++2e-→Cu E2θ=0.340V
求Cu(OH)2在298K时的活度积().
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“利用下列电极反应在298K时的标准电极电势:Cu(OH)2+2e-→Cu+2OH- E1θ=-0”相关的问题
更多“利用下列电极反应在298K时的标准电极电势:Cu(OH)2+2e-→Cu+2OH- E1θ=-0”相关的问题
某电极的电极反应为:
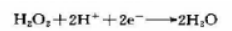
试求算25℃时该电极的标准电极电势φθ.已知水的离子积Kmθ=a(H+)a(OH-)=10-14.电极反应为:
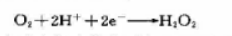
的电极和氧电极的标准电极电势分别为0.680V和0.401V.
A.电极的标准电极电势等于其绝对电极电势
B.电极的标准电极电势等于0
C.电极的标准电极电势是其室温时的电极电势
D.电极的标准电极电势以标准氢电极为参照标准
电池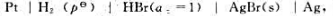 请:
请:
(1)写出电极反应与电池反应:
(2)若电池的电动势E/V=0.07131-4.99×10-6×(T/K-298),求正极在298K时的标准电极电势Eθ及电池反应的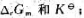
(3)判断此电池在298K时吸热还是放热,为什么?
(4)若HBr的浓度b=0.1mol·kg-1,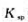 =1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
=1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
A.平衡电极电位
B.标准电极电位
C.非平衡电极电位
D.过电位

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
