 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列原电池:(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;(2)计算各电池的标
已知下列原电池:
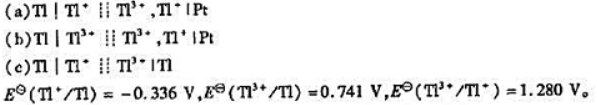
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的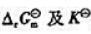 .
.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列原电池:
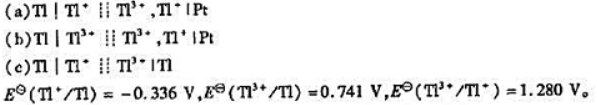
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的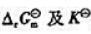 .
.
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“已知下列原电池:(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;(2)计算各电池的标”相关的问题
更多“已知下列原电池:(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;(2)计算各电池的标”相关的问题
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势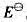 。
。
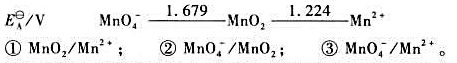
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势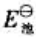 和电池反应的
和电池反应的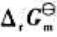 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势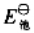 和电池反应的
和电池反应的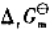 。
。
5.写出下列原电池的电极反应式和电池反应式,并计算25℃时原电池的电动势。
Fe|Fe2+(1.0mol/L)||Cl-(1.0mol/L)|Cl2(100kpa),Pt
将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?
已知 时,锰的元素电位图 (
时,锰的元素电位图 (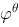 / V):
/ V):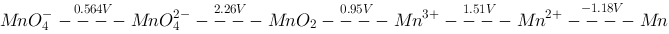 (1) 指出哪些物质在酸性溶液中会发生歧化反应; (2) 求
(1) 指出哪些物质在酸性溶液中会发生歧化反应; (2) 求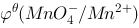 ; (3) 写出用电对
; (3) 写出用电对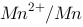 与标准氢电极组成原电池的电池符号及该电池的自发反应的方程式。
与标准氢电极组成原电池的电池符号及该电池的自发反应的方程式。
根据下列原电池反应,分别写出各原电池中正、负电极的电极反应(需配平)。 (1)Zn+Fe2+=Zn2++Fe (2)2I-+2Fe3+=I2+2Fe2+ (3)Ni+Sn4+=Ni2++Sn2+ (4)5Fe2++8H++MnO4-=Mn2++5Fe3++4H2O
现有原电池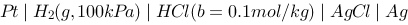 ,已知298K时,
,已知298K时,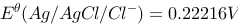 ,0.1mol/kg的HCl溶液的离子平均活度系数
,0.1mol/kg的HCl溶液的离子平均活度系数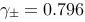 。(1)请写出电极反应和电池反应;(2)计算该电池的电动势
。(1)请写出电极反应和电池反应;(2)计算该电池的电动势
根据下列反应组成电池
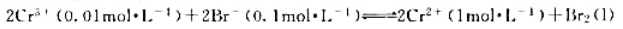
(1)写出电池符号;
(2)计算298K时的电动势,并判断反应自发进行的方向;
已知
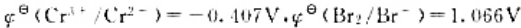
计算下列电池各电极的电极电势和电池电动势,并写出电池反应方程式:
(1)(—)Pt|H2(100kPa)|H+(2.0mol·L-1)||Cl-(1mol·L-1)|AgCl|Ag()
(2)(—)Pt|Sn2+(0.1mol·L-1),Sn4+(1mol·L-1)||Cl-(0.1mol·L-1)|Cl2(100kPa)|Pt()
(3)(—)Cu|Cu2+(0.1mol·L-1)||Cu2+(1.0mol·L-1)l Cu()
将下列反应设计成原电池,并应用教材中表7.7.1的数据计算25℃时电池反应的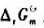 及
及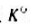 .
.
(1)2Ag++H2(g)=2Ag+2H+
(2)Cd+Cu2+=Cd2++Cu
(3)Sn2++Pb2+=Sn4++Pb
(4)2Cu+=Cu+Cu2+
A.A.电子得失数不间
B.B.组成原电池后,电池的电动势相同
C.C.反应的#图片3$#不同
D.D.组成原电池后,铜作原电池的正极

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
