 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电对 I2/I-的jϴ = 0.534V,当温度为298.15K,c(I-)=0.1 mol·dm-3时,j (I2/I-)等于多少?
A.0.534V
B.0.650V
C.0.593V
D.0.471V
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有4位网友选择 B,占比40%
- · 有3位网友选择 D,占比30%
- · 有2位网友选择 A,占比20%
- · 有1位网友选择 C,占比10%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.534V
B.0.650V
C.0.593V
D.0.471V
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“电对 I2/I-的jϴ = 0.534V,当温度为298.15K,c(I-)=0.1 mol·dm-3时,j (I2/I-)等于多少?”相关的问题
更多“电对 I2/I-的jϴ = 0.534V,当温度为298.15K,c(I-)=0.1 mol·dm-3时,j (I2/I-)等于多少?”相关的问题
298K时,在某一电导池中充以浓度为0.01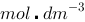 、电导率为0.14114
、电导率为0.14114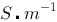 的KCl溶液,测得其电阻为525 Ω。若在该电导池内充以0.10
的KCl溶液,测得其电阻为525 Ω。若在该电导池内充以0.10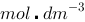 的
的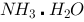 溶液时,测得电阻为2030 Ω,已知此时所用水的电导率为
溶液时,测得电阻为2030 Ω,已知此时所用水的电导率为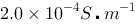 。试求: (1)该
。试求: (1)该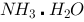 溶液的解离度; (2)若该电导池内充以纯水时的电阻值。
溶液的解离度; (2)若该电导池内充以纯水时的电阻值。
下列电池可用来测定溶液B中Ca2+的浓度。
Hg(l)|Hg2Cl2(s)|KCl(1mol·kg-1)||溶液B|CaC2O4(s)|Hg2C2O4(s)|Hg若用加入NaNO3的方法保持溶液B的离子强度为0.1mol·kg-1,当溶液B中含有0.01mol·kg-1Ca(NO3)2,在298K时测得电池的电动势E1为0.3243V;当溶液B中含Ca2+量不同时,于同样温度下测得E2为0.3111V。
已知273K时Weston标准电池的电池电动势的温度系数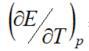 = -0.00004 V∙K-1,则ΔrSm=_____________J∙ K-1∙mol-1 (用普通计数法, 保留两位小数)
= -0.00004 V∙K-1,则ΔrSm=_____________J∙ K-1∙mol-1 (用普通计数法, 保留两位小数)
A、0.73V
B、0.89V
C、1.32V
D、1.49V
将下列反应组成原电池(温度为298.15K):2Fe3++Cu====2Fe2++Cu2+
(1)计算原电池的标准电动势;(2)写出其电池符号;(3)指出正极、负极,并写出电极反应;(4)当Cu2+的浓度升到10mol·L-1时,原电池的电动势为多少?
A、(1) (4) (5)
B、(2) (3) (5)
C、(2) (3) (4)
D、(2) (3)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
