 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
原则上只要知道了有关分子的结构,就可以用艾林方程计算反应速率常数k,而不必进行动力学测定。所以过渡状态理论有时称为绝对反应速率理论。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“原则上只要知道了有关分子的结构,就可以用艾林方程计算反应速率常数k,而不必进行动力学测定。所以过渡状态理论有时称为绝对反应速率理论。”相关的问题
更多“原则上只要知道了有关分子的结构,就可以用艾林方程计算反应速率常数k,而不必进行动力学测定。所以过渡状态理论有时称为绝对反应速率理论。”相关的问题
氧化亚氮的分解反应可按二级速率方程进行
2N2O→2N2+O2
在895℃时正反应速率常数k为977cm3/(mol·s),逆反应速率可以忽略。初始压力为0.10133MPa,反应开始时反应器中全为N2O。试计算在间歇反应器中时间为1.0s、10s及10min时的分解率。
A、反应速率常数由大到小变化
B、反应速率常数不变
C、反应级数由二级变为一级
D、反应级数由一级变为二级,反应速率常数由小变大
高温时NO2分解为NO和O2,其反应速率方程为
-v(NO2)=kc2(NO2)
在592K时,速率常数是4.98×10-1L·mol-1·s-1;在656K时,其值变为 4.74L·mol-1·s-1,计算该反应的活化能。
A、3rA=rB=2rP
B、6rA=3rB=2rP
C、rA=3rB=2rP
D、6rA=2rB=3rP

的反应级数、得到如下初始反应速率与反应物初始浓度关系的实验数据。
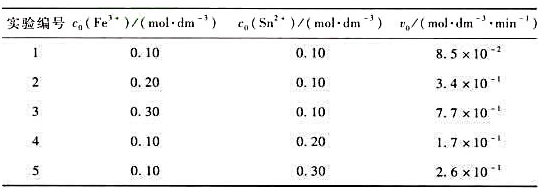
试计算反应对于Fe3+和Sn3+的反应级数;写出反应的速率方程并求出速率常数。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
