 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
提问人:网友wjl200508
发布时间:2022-01-06
[主观题]
1000 K 时将0.631 g 光气(COCl2)置于 0.472 dm3 真空容器中,达平衡后测得其总压为220 kPa,则反应 COCl2 (g)=== CO(g)+ Cl2(g) 在该温度下的平衡常数
1000 K 时将0.631 g 光气(COCl2)置于 0.472 dm3 真空容器中,达平衡后测得其总压为220 kPa,则反应 COCl2 (g)=== CO(g)+ Cl2(g) 在该温度下的平衡常数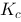 为 。
为 。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 抱歉!暂无答案,正在努力更新中……
抱歉!暂无答案,正在努力更新中……

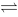 PCl3(g)+Cl2(g)此反应的Kp是
PCl3(g)+Cl2(g)此反应的Kp是

 2 NH3 ( g ) ,在673 K时
2 NH3 ( g ) ,在673 K时 ,在473K时,
,在473K时, 。则873 K时,
。则873 K时, = 。
= 。




























