 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1000mol/L NaOH滴定25.00mL 0.1000mol/L HCl,若以甲基橙为指示剂,滴定至pH=4.0为终点,则终点误差(TE)为( )
A.-0.10%
B.-0.20%
C.+0.20%
D.0.10%
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有1位网友选择 C,占比100%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.-0.10%
B.-0.20%
C.+0.20%
D.0.10%
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“用0.1000mol/L NaOH滴定25.00mL 0.1000mol/L HCl,若以甲基橙为指示剂,滴定至pH=4.0为终点,则终点误差(TE)为”相关的问题
更多“用0.1000mol/L NaOH滴定25.00mL 0.1000mol/L HCl,若以甲基橙为指示剂,滴定至pH=4.0为终点,则终点误差(TE)为”相关的问题
A .
用0.1000mol/L NaOH滴定含有0.10mol/L NH4Cl和0.1000mol/L HCl混合溶液中的HCl,宜采用的指示剂为( )。
A.甲基橙 B.甲基红 C.酚酞 D.二甲酚橙
A、NaOH+NaHCO3
B、NaHCO3+Na2CO3
C、NaOH
D、Na2CO3
称取仅含弱酸盐NaA和NaB的Na2CO3试样0.6125g,加水溶解后,以甲基橙为指示剂,用浓度为0.2000mol/L HCl标准溶液滴定,甲基橙变色时,消耗HCl标准溶液32.72mL;上述等量样品加水溶解后,若以酚酞为指示剂,用0.1000mol/L HCl标准溶液滴定,消耗25.34mL。(1)写出有关反应方程式;(2)各组分的质量分数是多少?(已知:弱酸HA的pKa=7.0,弱酸HB的pKa=1,MNa2CO3=105.99,MNaA=182.03,MNaB=132.0)
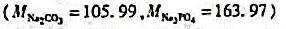
A. NACN(HCN的KA=4.9×10-10)
B. (CH2)6N4(KB=1.4×10-9)
C. NH3(pKB、=4.75)
D. NA2SiO3(H2SiO3的pK1=9.8,pK2=11.8)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
