 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在21.8℃时,反应NH4HS(s)=NH3(g)+H2S(g)的标准平衡常数。平衡混合气体的总压为()kPa。
在21.8℃时,反应NH4HS(s)=NH3(g)+H2S(g)的标准平衡常数
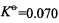 。平衡混合气体的总压为()kPa。
。平衡混合气体的总压为()kPa。
A.7.0
B.26
C.53
D.0.26
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在21.8℃时,反应NH4HS(s)=NH3(g)+H2S(g)的标准平衡常数
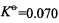 。平衡混合气体的总压为()kPa。
。平衡混合气体的总压为()kPa。
A.7.0
B.26
C.53
D.0.26
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“在21.8℃时,反应NH4HS(s)=NH3(g)+H2S(g)的标准平衡常数。平衡混合气体的总压为()kPa。”相关的问题
更多“在21.8℃时,反应NH4HS(s)=NH3(g)+H2S(g)的标准平衡常数。平衡混合气体的总压为()kPa。”相关的问题
在21.8℃时,反应NH4HS(s) NH2(g)+H2S(g)的标准平衡常数KΘ=0.070。平衡混合气体的总压为()kPa。
NH2(g)+H2S(g)的标准平衡常数KΘ=0.070。平衡混合气体的总压为()kPa。
A.7.0
B.26
C.53
D.0.26
NH4HS(s)受热时按下式发生分解反应:

在300.15K时,与NH4HS固体达平衡时的气体总压是66.46kPa。若该温度下NH4HS固体在一密闭容器中分解时,其中已有压力为45.45kPa的H2S存在,求平衡时各气体的分压。
固态NH4HS按下列反应建立平衡:
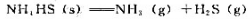
在一密闭容器型加进NH4HS(s),在25℃下达到平衡后到平系统的总压是66.66kPa.当固态NH4HS在密闭容器分解时,其中已含有压力为45.59kPa的H2S(g),计算平衡时各气体的分压.
已知在下列系统中可发生反应: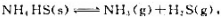 指出下列各系统的独立组分数和白由度数.
指出下列各系统的独立组分数和白由度数.
(1)25℃下由NH4HS(s),NH3(g)和H2S(g)组成的平衡系统.
(2)将NH4HS(s)放人抽空的密闭容器中形成的平衡系统.
(3)NH4HS(s)放人已有NH3(g)的密闭容器中构成的平衡系统.
反应NH4HS(s)=NH3(g)+H2S(g)的ΔrHmθ=94kJ·mol-1,ΔCp=0.298K时NH4HS(s)的分解压力为6.08X104Pa,(1)试计算308K时,NH4HS(s>的分解压力;(2>若将各为0.6mol的H2S(g)和NHa(g)放人20dm3容器中,试计算308K时生成NH4HS(s)为多少?
为40.0kPa的H2S,平衡后测得系统总压为77.8kPa;同样条件下,若将NH4HS(s)换成NH4Cl(s),平衡后测得系统总压为50.6kPa.试求:
(1)298K下两个分解反应的标准平衡常数和分解压力.
(2)298K下,将过量NH4HS(s)和NH4CI(s)同时置于抽空密闭容器中,达平衡时反应系统的总压.假设这两种盐类不形成固溶体.
A.0.0627
B.0.1026
C.0.1354
D.0.0513
下列反应中,
(A) CO(g)+Cl2(g)→COCl2(g) (B) 2NO2(g)→N2O4(g)
(C) NH4HS(s)→NH3(g)+H2S(g) (D) 2HBr(g)→H2(g)+Br2(l)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
