 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在酸性介质中,,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还
已知在酸性介质中,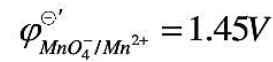 ,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还原电势与其条件电势间的关系。
,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还原电势与其条件电势间的关系。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在酸性介质中,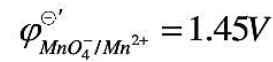 ,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还原电势与其条件电势间的关系。
,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还原电势与其条件电势间的关系。
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 更多“已知在酸性介质中,,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还”相关的问题
更多“已知在酸性介质中,,MnO4-被还原至一半时,体系的电势(半还原电势)为多少?试推出对称电对的半还”相关的问题
分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O7在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说明什么?(已知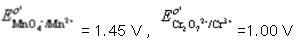 。)
。)
A.酸性介质中,溴元素中间价态的物质均易发生歧化
B.酸性介质中,HBrO能发生歧化
C.酸性介质中,BrO 4 - 能将Br - 氧化为BrO 3 -
D.酸性介质中,溴的含氧酸根都具有较强的氧化性
A..酸性介质中,溴元素中间价态的物质均易发生歧化
B.酸性介质中, HBrO能发生歧化
C.酸性介质中, BrO 4 - 能将 Br - 氧化为 BrO 3 -
D.酸性介质中,溴的含氧酸根都具有较强的氧化性
氯元素在酸性介质中的电势图为 HClO_____1.611V____Cl ____1.358V______Cl
____1.358V______Cl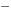 因为
因为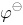 (HClO/Cl
(HClO/Cl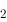 )>
)>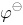 (Cl
(Cl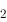 /Cl
/Cl ),所以Cl
),所以Cl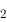 能发生歧化反应。()
能发生歧化反应。()
已知以下标准电极电势:

①画出酸性介质中铀的元素电势图;
②预测哪个氧化态最稳定;
③预测哪些氧化态会发生歧化反应;
④哪些氧化态在空气中不稳定?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
