 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
原电池 (-)Pt︱Fe 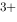 (1 mol·L
(1 mol·L 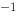 ),Fe
),Fe 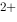 (1 mol·L
(1 mol·L 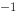 )‖Ce
)‖Ce 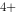 (mol·L
(mol·L 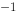 ) ,Ce
) ,Ce 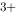 (mol·L
(mol·L  ) ︱Pt() 的电池反应是()。
) ︱Pt() 的电池反应是()。
A.Ce 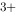 + Fe
+ Fe 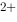 = Ce
= Ce 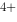 + Fe
+ Fe 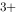
B.Ce 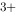 + Fe
+ Fe 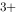 = Ce
= Ce 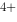 + Fe
+ Fe 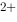
C.Ce 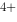 + Fe
+ Fe 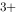 = Ce
= Ce 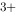 + Fe
+ Fe 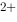
D.Ce 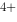 + Fe
+ Fe 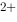 = Ce
= Ce 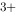 + Fe
+ Fe 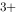
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有5位网友选择 C,占比50%
- · 有3位网友选择 B,占比30%
- · 有2位网友选择 A,占比20%




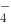


 + Zn=Sn
+ Zn=Sn + Zn
+ Zn 构成原电池,其电池符号为( )。
构成原电池,其电池符号为( )。 (c
(c )‖Sn
)‖Sn (c
(c )︱Sn
)︱Sn ( c
( c ) (+)
) (+) (Fe
(Fe /Fe)= -0.4402V, φ
/Fe)= -0.4402V, φ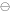 (Fe
(Fe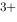 /Fe
/Fe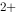 ) = 0.770V,故Fe
) = 0.770V,故Fe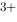 与Fe
与Fe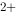 可以发生氧化还原反应;
可以发生氧化还原反应; /H
/H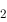 O
O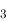 / Fe(OH)
/ Fe(OH)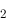
 /MnO
/MnO
 /Cr
/Cr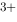
 值最大者为( )。
值最大者为( )。 / Ag)
/ Ag) )
)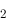 ]
] / Ag }
/ Ag } O
O 中锰的氧化数为( )。
中锰的氧化数为( )。



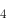 溶液时,加入铁钉可以防止Fe
溶液时,加入铁钉可以防止Fe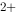 变成Fe
变成Fe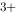 。( )
。( ) 0.153VCu
0.153VCu 0.521VCu则:Cu
0.521VCu则:Cu 与 Cu
与 Cu 在水溶液中的稳定性大小为( )。
在水溶液中的稳定性大小为( )。 大,Cu
大,Cu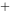 小
小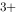 (1 mol·L
(1 mol·L )‖Ag
)‖Ag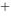 (1 mol·L
(1 mol·L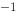 )︱Ag(+)中,若向铁半电池中加入适量的NaF溶液,则会使电动势增高。( )
)︱Ag(+)中,若向铁半电池中加入适量的NaF溶液,则会使电动势增高。( )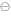 (Fe
(Fe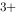 / Fe
/ Fe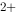 )=0.771V,φ
)=0.771V,φ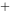 / Ag)=0.7996V,则Ag+Fe
/ Ag)=0.7996V,则Ag+Fe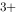 =Ag
=Ag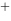 +Fe
+Fe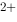 的标准平衡常数为( )。
的标准平衡常数为( )。




























