 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度时在CCl4溶液中发生N2O5的分解反应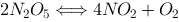 ,2.10 mol/L N2O5反应10 min后其浓度为1.30mol/L ,则这段时间内反应的平均速率为()
,2.10 mol/L N2O5反应10 min后其浓度为1.30mol/L ,则这段时间内反应的平均速率为()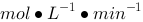 。
。
A.0.40
B.0.80
C.0.04
D.0.08
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有6位网友选择 A,占比31.58%
- · 有4位网友选择 D,占比21.05%
- · 有3位网友选择 B,占比15.79%
- · 有3位网友选择 C,占比15.79%
- · 有2位网友选择 C,占比10.53%
- · 有1位网友选择 D,占比5.26%



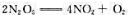 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算: 试计算: (1)在0~2.0 min内的平均反应速率:△c(O2)/△t=? (2)在第2.0 min时的瞬时速率:-dc(N2O5)/dt=? (3) N2O5浓度为1.00 mol.dm-3时的初速率:~dc(N2O5)/dt=?
试计算: (1)在0~2.0 min内的平均反应速率:△c(O2)/△t=? (2)在第2.0 min时的瞬时速率:-dc(N2O5)/dt=? (3) N2O5浓度为1.00 mol.dm-3时的初速率:~dc(N2O5)/dt=?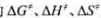 。
。
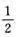 +O2(g),测得N2O5的分解速率常数为0.292min-1,反应的活化能为103kJ·mol-1,计算15℃时此反应的k及t1/2.
+O2(g),测得N2O5的分解速率常数为0.292min-1,反应的活化能为103kJ·mol-1,计算15℃时此反应的k及t1/2.




























