 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电对 Zn2+/Zn 的电极电势随以下哪种变化而增大?
A.c(Zn2+)减少
B.c(Zn2+)增大
C.锌片面积增大
D.三者都不是
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
- · 有6位网友选择 C,占比60%
- · 有3位网友选择 A,占比30%
- · 有1位网友选择 D,占比10%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.c(Zn2+)减少
B.c(Zn2+)增大
C.锌片面积增大
D.三者都不是
 参考答案
参考答案
 简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
简答题官方参考答案
(由简答题聘请的专业题库老师提供的解答)
 网友提供的答案
网友提供的答案
 更多“电对 Zn2+/Zn 的电极电势随以下哪种变化而增大?”相关的问题
更多“电对 Zn2+/Zn 的电极电势随以下哪种变化而增大?”相关的问题
1.以Pt为电极,电解含有Ag+(0.01moldm-3)和Cu2+(1mol dm-3)的硫酸盐。假定[H+]=1mol dm-3,已知氢在铂电极上的超电势为0.4V,氧在铂电极上的超电势为0.5V,求在阴极析出物质的先后顺序及开始析出物质时对应的槽压。 已知φϴAg+/ Ag = 0.799 V,φϴCu2+/ Cu = 0.337 V。 2. 298K时,欲回收电镀液中的银,废液中AgNO3浓度为10-6mol·L-1 ,还含有少量的Cu2+存在,若以石墨为阴极,银用阴极电解法回收,要求回收99%的银.计算中令活度系数γ1 =1。试计算:(1) Cu2+的浓度应低于多少?(2)阴极电位应控制在什么范围内?(3)什么情况下Cu与Ag同时析出? 3. 以惰性电极电解SnCl2的水溶液进行阴极镀Sn,阳极中产生O2,已知:αSn2+ = 0.10 , αH+ =0.010,阳极上ηO2 =0.50V,已知:φϴSn2+/Sn = -0.140V,φϴH+,H2O/O2 = 1.23V, (1)试写出电极反应,并计算实际分解电压,(2)若 φH2,阴=0.40V,试问要使αSn2+ 降低到何值时才开始析出氢? 注意:以上题目均不考虑氧分压。
A、电动势增大
B、电动势减小
C、电动势不变
D、无法确定
 。
。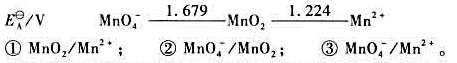
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的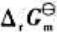 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的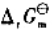 。
。
298.15K标准状态下,反应[Cu(CN)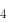 ]
]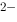 +4H
+4H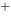 = 4HCN + Cu
= 4HCN + Cu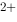 自发进行的方向应为( )。(已知298.15K时,
自发进行的方向应为( )。(已知298.15K时,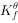
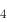 ]
]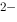 }=2.0×10
}=2.0×10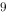 ,
,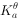
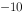 )
)
A、正向
B、逆向
C、平衡
D、三种情况都有可能
A、0.534V
B、0.650V
C、0.593V
D、0.471V
A、(1) (4) (5)
B、(2) (3) (5)
C、(2) (3) (4)
D、(2) (3)

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
